Polyethylenglykole in der Kosmetik – Wie schädlich ist PEG ?
Was sind Polyethylenglykole ?
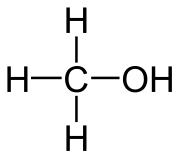
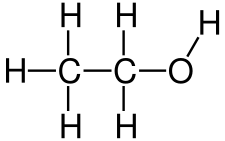
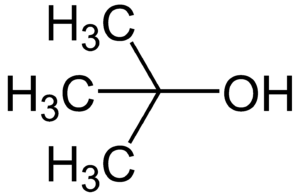
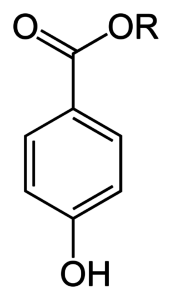
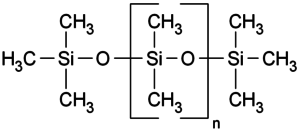
Polyethylenglykole (kurz PEG) sind Plastiken, sogenannte Polymere, welche in vielen Bereichen Anwendung finden. Sie bestehen aus langen Ether Ketten und haben viele nützliche Eigenschaften.
Wie sind sie Aufgebaut ?

Flüssiges PEG 400 Abb. 1
PEG entsteht, wenn man Ethylenoxid, ein hochgiftiges Gas, über alkalische oder saure Katalyse polymerisiert. PEG besitzt verschiedene Kettenlängen, welche ihm verschiedene Eigenschaften geben.
So sind z.B. Kettenlängen von :
-
200-400 g/mol flüssig
-
600 g/mol pastös
-
Und ab 3000 g/mol fest
Bei Kettenlängen zwischen 200 und 35.000 g/mol werden sie Polyethylenglykole genannt, ab einer Kettenlänge von 35.000 g/mol werden sie Polyethylenoxide genannt, da die -OH Gruppen an jeweils Anfang und Ende des Polymers vernachlässigt werden können.[1]
Wo wird PEG benutzt ?
PEG findet Anwendung in der Medizin, als Trägerstoff für Tabletten, Tropen und Dragees, sowie als Abführmittel und Gegengift für Flusssäure und Stickstofftriflourid Vergiftungen[2]. Ebenfalls wird es als Konservierungsstoff für Fossilien benutzt, um diese vor Umwelteinflüssen zu schützen[3], sowie als Gleit-, und Trennmittel in der Industrie[4]. Es wird als Weichmacher und Basis für Salben verwendet. Man findet es in der Kosmetik in Cremes, Lotion, Parfüms, Deodorants, Lippenstifte, Zahnpasten, Haarpflegeprodukten und Badezusätzen[5]. Zudem benutzt man es zu Schnelltrocknung von Edelhölzern.
Wieso wird PEG so häufig benutzt ?
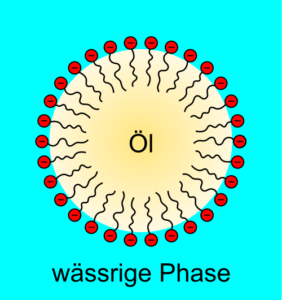
PEG ist sehr gut wasserlöslich, bis zu PEG 35.000 welches noch zu 50% mit Wasser gemischt werden kann, aufgrund dessen ist es ein gutes Trocknungs-, aber auch Feuchthaltemittel, sowie ein guter Emulgator[6]. Ebenfalls weist es eine sehr niedrige Toxizität auf, weshalb es seine medizinischen Anwendungen problemlos erfüllen kann[7]. Es ist bis zu einer molekularen Masse von 1500 biologisch Abbaubar. Ab einer Temperatur von 150°C zersetzt es sich[8].
Was ist das Problem mit PEG in Kosmetika ?
PEG macht die Haut durchlässiger, für Wirkstoffe von Kosmetika, aber auch für mögliche Giftstoffe. Wir haben Tag für Tag mit Giftstoffen zu tun, auch wenn wir davon nichts merken. Unser Körper schützt uns vor Bakterien, Viren aber auch Toxinen, und unsere Haut erfüllt diese Aufgabe dadurch, dass sie keine unerwünschten Stoffe in unseren Körper lässt. Fremdstoffe, welche unser Körper als Gefahr erkennt werden über Abwehrstoffe abgehalten in den Körper einzudringen. Hierfür weitet der Körper die Blutgefäße der entsprechenden Hautstelle, erhöht den Blutfluss und schickt Botenstoffe und Enzyme zur betroffenen Stelle. Dies macht sich als Reizung bzw. Rötung bemerkbar[9]. PEG schwächt die natürliche Barriere der Haut, wodurch diese Abwehrerscheinungen auftreten, jedoch um ein vielfaches weniger effektiv sind.[10] Unser Körper wehrt sich ebenfalls Tagtäglich gegen sogenannten oxidativen Stress und ionisierende Strahlungen d.h. In unsere Atmosphäre befinden sich freie Sauerstoffradikale (O-) und kurzwellige, hochenergetische Strahlen wie UV-Strahlen, welche die Haut angreifen. Diese werden über äußere Hautschichten und die natürliche Barriere, sowie Enzyme neutralisiert[11]. Sind diese Schutzmechanismen beschädigt, so können Radikale und Strahlungen die Haut schädigen, aber auch tiefer in das Gewebe eindringen, und dort gar für Krebs sorgen[12].

Abb. 2
Gibt es Alternativen ?
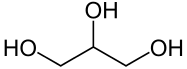
Ja es gibt Alternativen, sogar welche, bei denen man nicht in der Natur suchen muss. Eines der, im Moment am vielversprechendsten, ist das 2,4-Polysarcosine. Es ist 100% biologisch abbaubar, nicht toxisch, nicht reizend, rötend oder Immunsystem beeinflussend. Sie sind synthetisch, können deshalb maßgeschneidert werden, und zum jetzigem Stande haben sie viele Variationsmöglichkeiten[13]. Eine natürliche Alternative ist das Propandiol, welches aus Maissirup hergestellt werden kann. Es hat ähnliche wasserlöslichen Eigenschaften, kann ebenfalls als Tensid für Emulsionen benutzt werden, und ist nicht Toxisch. Zudem fördert es die Resorption von Wirkstoffen ohne die Hautbarriere zu schädigen, und wirkt antimikrobiell, weshalb Konservierungsstoffe überflüssig werden[14].
–
Quellen zum Nachlesen:
Wissenschaftlicher Artikel über 2,4-Polysarcosine als Alternative zu PEG [13]
Greenpeace Statement zu PEG [8]
Wissenschaftlicher Artikel zu 1,2 Propendiol [14]
Artikel zu Polyethylenglykol [10][11][12]
Wikipedia[1][2][3][4][5][6][7][9]